实验室李斌课题组发现FOXP3+Treg细胞体内功能稳定性调节新通路
11月18日,国际学术期刊
调节性T(Treg)细胞维持着体内免疫稳态,抑制过度激活的免疫反应。Treg细胞的稳定性与可塑性关系到多种免疫性疾病的发生和发展。其中,Treg细胞功能稳定性受到多种胞外信号调节,例如细菌脂多糖(LPS)、IL-1β和热激活(heat shock)等信号能诱导Treg细胞关键转录因子FOXP3蛋白的泛素化降解。但是,体内调控FOXP3+Treg细胞稳定性的机制目前尚不清楚。
分子免疫学课题组博士研究生李扬扬和上海中医药大学药学院吕玥博士在李斌研究员的指导下,利用Treg细胞中特异性敲除去泛素化酶Usp21基因的小鼠,发现小鼠肝脏、肺和唾液腺等器官中Usp21基因缺陷的Treg细胞分泌大量的炎症因子IFN-γ。体外分化实验也证实该细胞变得更像I型辅助性T(Th1)细胞。进一步研究发现,USP21通过去泛素化修饰来抑制关键转录因子FOXP3蛋白的降解,从而稳定Treg细胞。因此,在体内,FOXP3不稳定的Treg细胞具有分泌大量Th1型细胞因子的能力,并进一步诱发过度激活的后续Th1型免疫反应。近期研究成果显示,结肠癌患者体内低表达FOXP3的Treg细胞分泌更多的炎性细胞因子IFN-γ,并预示结肠癌患者更好存活率。因此,针对去泛素化酶USP21的小分子抑制剂有可能会在肿瘤微环境中诱导产生更多的Th1-like Treg细胞,更有利于打破肿瘤微环境中的免疫耐受,增强抗肿瘤免疫反应。
该课题获得科技部973项目、国家基金委面上项目、重点项目及杰青项目、中科院分子细胞卓越中心及细胞命运可塑性先导项目B、上海市优秀学术学科带头人(A类)、上海市免疫学研究所余㵑基金会等经费支持。
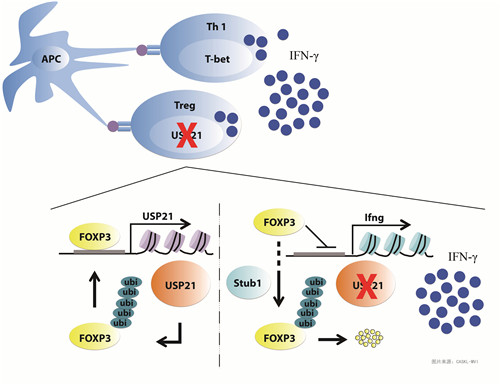
去泛素化酶USP21抑制Th1-like Treg细胞的产生