2021年1月8日,国际学术期刊Science Advances在线发表了中国科学院上海巴斯德研究所钟劲课题组与北京大学魏文胜课题组合作研究论文“TRIM26 is a critical host factor for HCV replication and contributes to host tropism”。
丙肝病毒(HCV)是一种RNA病毒,属于黄病毒科的丙肝病毒属。60-80%的HCV感染者会发展成为慢性丙肝,导致严重的肝脏疾病,例如肝硬化以及肝癌。近年来开发的直接抗病毒药物(DAA)极大地提高了丙肝的治疗效率,但是由于缺乏疫苗,HCV的彻底清除仍然具有很大的挑战性。HCV动物感染模型对于丙肝疫苗研发至关重要。HCV只感染人和黑猩猩,但是由于伦理等问题,现在已经禁止使用黑猩猩作为模型动物。表达HCV受体分子的转基因小鼠能有限支持HCV感染,但由于缺少其它人源宿主因子,尤其是针对病毒进入细胞之后的关键步骤的宿主因子,该转基因小鼠模型在丙肝疫苗效价评价的应用上仍然非常有限。因此鉴定新的种属特异性HCV宿主因子对于HCV小动物感染模型的建立具有非常重要的意义。
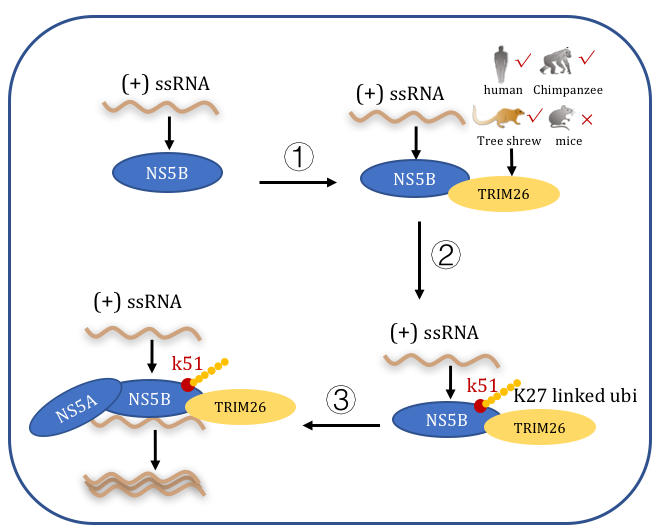
在该研究中,科研人员通过全基因组CRISPR/Cas9筛选首次发现E3泛素化连接酶TRIM26是HCV重要的宿主因子。实验结果显示TRIM26特异性地促进了HCV基因组的复制,而对于同属黄病毒科的其它病毒(如登革病毒和寨卡病毒)的复制没有作用。机制研究发现TRIM26与病毒编码的RNA依赖性RNA复制酶NS5B相互作用,催化NS5B蛋白的第51位赖氨酸发生K27连接的泛素化修饰,从而增强NS5B与病毒复制复合体中另外一个关键蛋白NS5A的结合,最终促进HCV基因组的复制。该研究还比较了不同宿主来源的TRIM26对于HCV复制的影响,发现人以及树鼩来源的TRIM26可以支持病毒的复制,但是小鼠来源的TRIM26不能支持HCV复制。序列分析发现与其它种属相比,鼠源TRIM26存在一段6个氨基酸的插入,删除掉该氨基酸插入序列的鼠源TRIM26可以部分恢复其与病毒NS5B的相互作用及帮助病毒基因组复制的功能。最后该研究还发现在小鼠肝细胞中表达人源TRIM26可以显著增强HCV的感染效率。该项研究不但发现了HCV新的宿主因子,进一步解析了HCV复制的分子机制,还为HCV小动物感染模型的建立提供了一个新的思路,具有重要的科学意义。
图注:TRIM26帮助HCV基因组复制的模式图
该研究得到了中国科学院战略性先导科技专项(先导B),国家自然科学基金以及中国科学院西部之光等项目的资金支持。上海巴斯德研究所与上海科技大学联培博士研究生梁轶莎,中山大学中山医学院张桂根副教授以及北京大学博士研究生李齐恒为本文并列第一作者。上海巴斯德研究所钟劲研究员,北京大学生命科学学院魏文胜教授以及张桂根副教授为本文共同通讯作者。清华大学丁强课题组也参与了本项研究。
全文链接:https://advances.sciencemag.org/content/7/2/eabd9732