诊断中心建立适于病毒检测的新荧光PCR方法
近期,中国科学院上海巴斯德研究所病原诊断中心建立了一种基于高保真酶和HF探针的新型荧光定量方法,有效地解决了高变异对病毒诊断的影响,极大地突破了病毒性传染病诊断的最大瓶颈,使病毒检测的灵敏性和广谱性得到了大幅度的提升。研究结果“A novel quantitative PCR mediated by high-fidelity DNA polymerase”(一种高保真酶介导的新型荧光定量方法)于9月4日发表在国际学术期刊Scientific Reports上。
传染病严重威胁人类健康,超过70%的新发突发传染病由病毒造成。与其他病原体相比,病毒最大的特点在于其高变异性,这成为病毒检测的最大挑战。高变异会严重干扰检测结果的准确性、影响检测的灵敏度、增加引物和探针的设计难度。因此较难获得高变异病毒的高广谱和高灵敏的检测方法。现有的PCR、qPCR及各种恒温扩增方法(如LAMP,RPA等)均不能很好解决病毒高变异性对检测的影响。
为了解决高变异对病毒检测影响的问题,上海大学联合培养硕士研究生张梦玲,在导师张驰宇研究员的指导下,建立了一种基于高保真酶的新荧光PCR方法。该方法使用HFman探针,依赖高保真聚合酶的3’-5’外切酶活性,可以高效切除探针3’荧光标记的碱基,启动扩增。无论探针(或引物)3端是否存在与模板的错配,聚合酶均可以高效地启动扩增,不受错配影响,因此可以容忍突变模板(图1)。与传统TaqMan探针法相比,该方法只需要一个HFman探针和一条对应引物,设计相对简单。为了验证方法的可靠性,我们建立了HIV-1病毒载量测定的方法。为了检测方法的灵敏性和可靠性,我们选择了21个HIV阳性的临床样品(覆盖高、中和低病毒载量),同时用新方法和罗氏的最新款HIV-1病毒载量试剂盒(COBAS® AmpliPrep /COBAS® TaqMan® HIV-1 Test,v2.0)进行了比较,结果显示新方法与罗氏的试剂盒检测结果具有很好的一致性(图2),表明了新方法和HIV-1定量检测方法具有良好的商业化开发前景。
除了用于病毒检测外,稍加改进,该方法也可以用于突变(SNP)的检测,目前该方法已申请了2项专利。
该研究得到了上海市疾病预防控制中心钟平教授、林悦博士,以及上海巴斯德研究所金侠教授的大力帮助和支持。项目获得了国家传染病重大专项和国家自然科学基金等项目的资助。
文章链接:www.nature.com/articles/s41598-017-10782-4
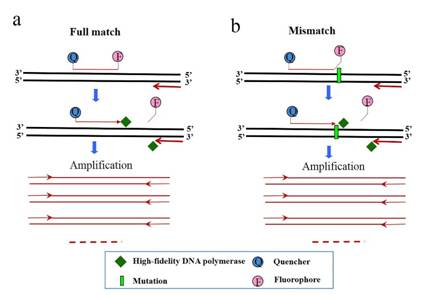
图1.原理图
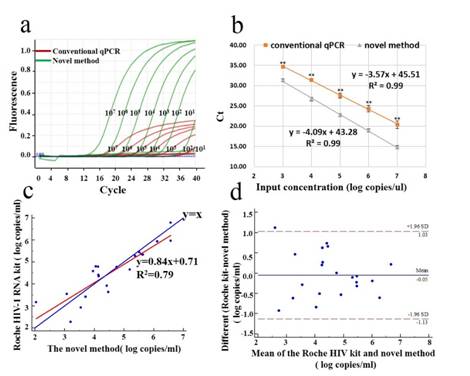
图2. HIV-1病毒载量检测方法及罗氏试剂盒比较.(a和b)标准曲线(HIV-1 RNA:107-100copies/ul);(c和d)与Roche HIV-1 kit的比较。