黄忠研究组在丙型肝炎病毒基因工程疫苗研发中取得突破
近期,实验室黄忠课题组与钟劲课题组合作,在丙型肝炎病毒(hepatitis C virus, HCV)疫苗研究中取得突破性进展。研究成果“Altered glycosylation patterns increase immunogenicity of a subunit HCV vaccine inducing neutralizing antibodies which confer protection in mice”(糖基化类型的改变增强丙型肝炎病毒亚单位疫苗的免疫原性及保护性中和抗体的诱导能力)于9月17日在国际学术期刊Journal of Virology在线发表。
HCV感染是慢性肝炎的主要病因之一。目前在全球已经有超过 1亿7千万 HCV 感染病例,感染率为 3%,并且每年有 30万 到 40 万新发病例。在我国, HCV 感染率为 3.2%。病人感染 HCV 后 80%转为慢性感染,慢性感染病人中 10%-20%转归为肝硬化, 1%-5%转归为肝癌。 治疗性药物聚乙二醇干扰素联合利巴韦林只能治愈约50%的病人,尤其对 1 型 HCV 感染治疗效果较差;新一代药物Direct-antiviral agents (DAAs)的上市,将治愈率提高到 90%以上,但新药价格极其昂贵、而且存在产生耐药的可能。因此,研制安全有效的预防性HCV 疫苗对于减轻这一全球性公共卫生负担、彻底解决丙肝问题具有重要意义。然而,由于 HCV 基因组的高频突变、包膜蛋白的糖基化、病毒颗粒被脂类分子包裹、非中和性抗体干扰等因素的影响,如何诱导产生能够中和全部7个病毒亚型的抗体一直是HCV 疫苗研发的最大难点。目前还没有针对 HCV 的预防性疫苗上市。
为研制HCV基因工程疫苗,上海巴斯德所博士研究生李大鹏等在黄忠研究员和钟劲研究员的指导下,以HCV包膜蛋白E2为疫苗靶点,利用果蝇S2重组表达体系制备了了可溶性E2蛋白(sE2),并且系统地评价了sE2疫苗的免疫原性、诱导广谱中和抗体能力及其在小鼠感染模型上的保护作用。结果表明,该sE2疫苗免疫小鼠能够诱导出针对全部7个亚型HCV的广谱中和抗体,更重要的是,上海巴斯德所研究团队与美国普林斯顿大学Alexander Ploss教授合作,确定了sE2疫苗在人源化小鼠模型中能够有效预防HCV感染,具有良好的免疫保护效果。进一步的机制研究发现,昆虫细胞表达的sE2蛋白与来源于哺乳动物系统的抗原相比较,其糖基化类型更为简单,而这种简单糖基化修饰对于sE2有效诱导广谱中和抗体是至关重要的。该项目所研发的sE2亚单位疫苗在诱导广谱中和抗体方面优于目前处于临床试验阶段的HCV候选疫苗,而且该疫苗成分简单、产量高,因此具有很好的产业化前景。
该研究得到了中科院上海巴斯德所邓强研究员、神经科学研究所孙强研究员的科研支持,获得了科技部973、基金委、国家传染病重大专项 、中科院海外专家团队项目,以及美国国立健康研究院、美国癌症研究学会和Burroughs Wellcome Fund等经费的支持。
相关链接:https://www.ncbi.nlm.nih.gov/pubmed/27630242
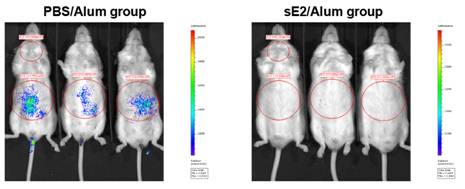
图片说明 重组sE2疫苗在人源化小鼠模型上能够预防HCV病毒感染。
(左)对照组小鼠;(右)sE2疫苗免疫小鼠。小鼠体内生物荧光信号的
强弱代表HCV病毒感染程度。